
విషయము
- దశల్లో
- విధానం 1 పిహెచ్ మీటర్ ఉపయోగించి
- విధానం 2 పొద్దుతిరుగుడు కాగితాన్ని ఉపయోగించండి
- విధానం 3 pH ను అర్థం చేసుకోవడం
నీటి pH ను విశ్లేషించడం చాలా ముఖ్యం (అనగా దాని ఆమ్లత లేదా క్షారత స్థాయి). మనం ఆధారపడిన మొక్కలు మరియు జంతువులు నీటిని వినియోగిస్తాయి మరియు ప్రతిరోజూ నేరుగా తినేస్తాము. నీటి యొక్క pH సంభావ్య కాలుష్యానికి ఆధారాలు అందిస్తుంది. అందువల్ల, నీటి pH విశ్లేషణ ఒక ముఖ్యమైన ప్రజారోగ్య కొలత.
దశల్లో
విధానం 1 పిహెచ్ మీటర్ ఉపయోగించి
-

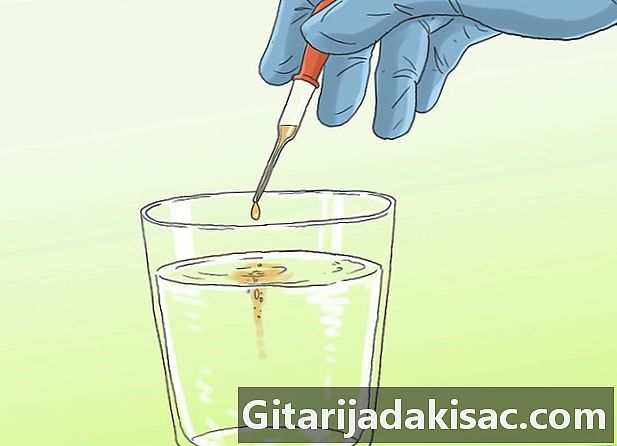
తయారీదారు సూచనల ప్రకారం ప్రోబ్ మరియు మీటర్ను క్రమాంకనం చేయండి. దీన్ని క్రమాంకనం చేయడానికి, మీరు తెలిసిన పిహెచ్ పదార్ధంతో మీటర్ను పరీక్షించాల్సి ఉంటుంది. మీరు ఈ కొలతల ఆధారంగా దాన్ని సర్దుబాటు చేయవచ్చు. మీరు ప్రయోగశాల వెలుపల నీటిని విశ్లేషించబోతున్నట్లయితే, మీరు ఫీల్డ్లోని పరికరాన్ని దెబ్బతీసే ముందు అమరికను చేయాలి.- ఉపయోగించే ముందు ప్రోబ్ను శుభ్రమైన నీటితో శుభ్రం చేసుకోండి. శుభ్రమైన గుడ్డతో ఆరబెట్టండి.
-

శుభ్రమైన కంటైనర్లో నీటి నమూనాను సేకరించండి.- ఎలక్ట్రోడ్ యొక్క కొనను కప్పడానికి నీటి నమూనా తగినంత లోతుగా ఉండాలి.
- ఉష్ణోగ్రత స్థిరీకరించడానికి సమయం ఉన్నందున నమూనాను కొద్దిసేపు విశ్రాంతి తీసుకోవడానికి అనుమతించండి.
- థర్మామీటర్తో నమూనా యొక్క ఉష్ణోగ్రతను కొలవండి.
-

నమూనా ఉష్ణోగ్రత ప్రకారం మీటర్ సెట్ చేయండి. ప్రోబ్ యొక్క సున్నితత్వం నీటి ఉష్ణోగ్రత ద్వారా ప్రభావితమవుతుంది మరియు మీరు ఉష్ణోగ్రత డేటాను నమోదు చేయకపోతే సూచించిన కొలత మంచిది కాదు. -

ప్రోబ్ను నమూనాలో ఉంచండి. మీటర్ సమతుల్యం కోసం వేచి ఉండండి. కొలత స్థిరంగా ఉన్నప్పుడు ఇది చేరుకుంటుంది. -

నమూనా యొక్క pH కొలతను చదవండి. మీ పిహెచ్ మీటర్ మీకు 0-14 స్కేల్పై కొలత ఇవ్వాలి. నీరు స్వచ్ఛంగా ఉంటే, కొలత 7 కి దగ్గరగా ఉండాలి. మీ రికార్డులను రాయండి.
విధానం 2 పొద్దుతిరుగుడు కాగితాన్ని ఉపయోగించండి
-

పిహెచ్ పేపర్ మరియు పొద్దుతిరుగుడు కాగితం మధ్య వ్యత్యాసాన్ని తెలుసుకోండి. పరిష్కారం యొక్క సరైన కొలతను పొందడానికి, మీరు pH కాగితాన్ని ఉపయోగించవచ్చు. ఇది ప్రస్తుత పొద్దుతిరుగుడు కాగితంతో అయోమయం చెందకూడదు. ఆమ్లాలు మరియు స్థావరాలను విశ్లేషించడానికి రెండింటినీ ఉపయోగించవచ్చు, కానీ అవి తీవ్రంగా భిన్నంగా ఉంటాయి.- పిహెచ్ బ్యాండ్లు సూచిక స్తంభాల శ్రేణిని కలిగి ఉంటాయి, ఇవి పరిష్కారాన్ని బహిర్గతం చేసిన తర్వాత రంగును మారుస్తాయి. ప్రతి కాలమ్ యొక్క ఆమ్లాలు మరియు స్థావరాల యొక్క తీవ్రత భిన్నంగా ఉంటుంది. అవి మారిన తర్వాత, రంగులను కిట్లో అందించిన ఉదాహరణలతో పోల్చవచ్చు.
- పొద్దుతిరుగుడు కాగితం ఒక ఆమ్లం లేదా బేస్ (ఆల్కలీన్) కలిగి ఉన్న కాగితపు కుట్లు కలిగి ఉంటుంది. అవి ఎక్కువ సమయం ఎరుపు రంగులో ఉంటాయి (అవి స్థావరాలతో స్పందించే ఆమ్లాన్ని కలిగి ఉంటే) లేదా నీలం (అవి ఆమ్లాలతో స్పందించే బేస్ కలిగి ఉంటే). పదార్ధం ఆల్కలీన్ అయితే ఎరుపు బ్యాండ్లు నీలం రంగులోకి వస్తాయి, ఒక ఆమ్లంతో సంబంధం కలిగి ఉంటే నీలిరంగు బ్యాండ్లు ఎరుపు రంగులోకి మారుతాయి.సన్ఫ్లవర్ పేపర్లను శీఘ్రంగా మరియు సులభంగా కొలవడానికి ఉపయోగించవచ్చు, కాని చౌకైనవి ఒక పరిష్కారం యొక్క pH యొక్క ఖచ్చితమైన కొలతను అనుమతించవు.
-

శుభ్రమైన కంటైనర్లో నీటి నమూనాను సేకరించండి. టేప్ కవర్ చేయడానికి నమూనా లోతుగా ఉండాలి. -

మీ నమూనాలో కాగితపు స్ట్రిప్ను ముంచండి. కొన్ని సెకన్ల ఎక్స్పోజర్ సరిపోతుంది. కాగితం యొక్క విభిన్న నిలువు వరుసలు కొన్ని క్షణాల్లో రంగును మార్చడం ప్రారంభిస్తాయి. -

విశ్లేషణ టేప్ ముగింపును కాగితంతో అందించిన రంగు గ్రాఫ్తో పోల్చండి. చార్టులోని రంగులు మీ బ్యాండ్లోని వాటికి సరిపోలాలి. ప్రతి రంగు pH కొలతతో సంబంధం కలిగి ఉండాలి.
విధానం 3 pH ను అర్థం చేసుకోవడం
-
ఆమ్లాలు మరియు స్థావరాలు ఎలా నిర్వచించబడతాయో కనుగొనండి. లాసిడిటీ మరియు క్షారతత్వం (స్థావరాలను వివరించడానికి ఉపయోగించే పదం) రెండూ హైడ్రోజన్ అయాన్లచే నిర్వచించబడతాయి, అవి అవి కోల్పోతాయి లేదా అంగీకరిస్తాయి. ఆమ్లం అనేది హైడ్రోజన్ అయాన్లను కోల్పోయే (లేదా కొన్ని ప్రకారం) ఇస్తుంది. -
పిహెచ్ స్కేల్ అర్థం చేసుకోండి. నీటిలో కరిగే పదార్థాల ఆమ్లత్వం లేదా క్షారత స్థాయిని అంచనా వేయడానికి పిహెచ్ సంఖ్య ఉపయోగించబడుతుంది. నీరు సాధారణంగా సమానమైన హైడ్రాక్సైడ్ (OH-) మరియు హైడ్రోనియం (H30 +) అయాన్లను కలిగి ఉంటుంది. నీటిలో ఒక ఆమ్ల లేదా ఆల్కలీన్ పదార్ధం కలిపినప్పుడు, ఇది హైడ్రాక్సైడ్ మరియు హైడ్రోనియం అయాన్ల నిష్పత్తిని మారుస్తుంది.- ఈ సంఖ్య సాధారణంగా 0 నుండి 14 స్కేల్లో ఉంటుంది (కొన్ని పదార్థాలు వాస్తవానికి ఈ పరిధికి మించి ఉండవచ్చు). తటస్థ పదార్ధాలకు 7 కి దగ్గరగా పిహెచ్, 7 కన్నా తక్కువ ఆమ్ల పదార్థాలు మరియు 7 పైన ఆల్కలీన్ పదార్థాలు ఉంటాయి.
- పిహెచ్ స్కేల్ లోగరిథమిక్, అంటే ఒక యూనిట్ యొక్క వ్యత్యాసం వాస్తవానికి ఆమ్లత్వం లేదా క్షారతలో 10 రెట్లు ఎక్కువ వ్యత్యాసం. ఉదాహరణకు, 2 యొక్క pH ఉన్న పదార్ధం వాస్తవానికి 10 రెట్లు ఎక్కువ ఆమ్లంగా ఉంటుంది, దీని pH 3 మరియు 100 రెట్లు ఎక్కువ ఆమ్లంగా ఉంటుంది. 4 pH ఉన్న పదార్ధం కంటే. స్కేల్ ఆల్కలీన్ పదార్థాలకు అదే విధంగా పనిచేస్తుంది, పదిరెట్లు వ్యత్యాసానికి అనుగుణంగా కొలత యూనిట్.
-

మేము నీటి pH ను ఎందుకు కొలవాలనుకుంటున్నామో తెలుసుకోండి. స్వచ్ఛమైన నీటిలో 7 pH ఉండాలి, కాని పంపు నీటిలో సాధారణంగా 5.5 మరియు 6 మధ్య pH ఉంటుంది. అధిక ఆమ్ల నీరు (తక్కువ pH తో) విష ఉత్పత్తులను కరిగించే అవకాశం ఉంది. ఇవి నీటిని కలుషితం చేస్తాయి మరియు మానవ వినియోగానికి అనర్హమైనవి.- సిటులో పిహెచ్ను కొలవడానికి సాధారణంగా ఇష్టపడతారు. మీరు ఒక ప్రయోగశాలలో అధ్యయనం కోసం నీటి నమూనాను సేకరిస్తే, నీటిలోని కార్బన్ డయాక్సైడ్ నీటిలో కరిగిపోతుంది. ఈ కరిగిన కార్బన్ డయాక్సైడ్ నీటిలో ఉన్న అయాన్లతో చర్య జరుపుతుంది మరియు ప్రాథమిక లేదా తటస్థ ద్రావణాల యొక్క ఆమ్లతను పెంచుతుంది. కార్బన్ డయాక్సైడ్ కలుషితాన్ని నివారించడానికి, మీరు సేకరించిన 2 గంటల కన్నా తక్కువ నీటిని కొలవాలి.